Il tasso di corrosione è un parametro multifattoriale che dipende sia dalle condizioni ambientali esterne che dalle proprietà interne del materiale. Nella documentazione normativa e tecnica, ci sono alcune restrizioni sui valori consentiti di distruzione dei metalli durante il funzionamento di apparecchiature e strutture edili per garantirne il funzionamento senza problemi. In ingegneria, non esiste un metodo universale per determinare il tasso di corrosione. Ciò è dovuto alla complessità di prendere in considerazione tutti i fattori. Il metodo più affidabile è studiare la cronologia delle operazioni della struttura.
Criteri

Attualmente, nella progettazione ingegneristica vengono utilizzati diversi tassi di corrosione:
- Secondo il metodo diretto di valutazione: riduzione della massa di una parte metallica per unità di superficie - indicatore di peso (misurato in grammi per 1 m2 per 1 ora); profondità del danno (o permeabilità del processo di corrosione), mm/anno; la quantità della fase gassosa rilasciata dai prodotti di corrosione; il periodo di tempo durante il quale compare il primo danno da corrosione; numero di centri di corrosione per unità di superficiesuperfici che sono apparse in un certo periodo di tempo.
- Stima indiretta: forza della corrente di corrosione elettrochimica; resistenza elettrica; cambiamento delle caratteristiche fisiche e meccaniche.
Il primo indicatore di valutazione diretta è il più comune.
Formule di calcolo
Nel caso generale, la perdita di peso che determina il tasso di corrosione del metallo si trova con la seguente formula:
Vkp=q/(St), dove q è la diminuzione della massa del metallo, g;
S - superficie da cui è stato trasferito il materiale, m2;
t - periodo di tempo, ore
Per la lamiera e i gusci ricavati da essa, determinare l'indice di profondità (mm/anno):
H=m/t, m è la profondità di penetrazione nel metallo.
C'è la seguente relazione tra il primo e il secondo indicatore sopra descritti:
H=8, 76Vkp/ρ, dove ρ è la densità del materiale.
Principali fattori che influenzano il tasso di corrosione
I seguenti gruppi di fattori influenzano il tasso di distruzione dei metalli:
- interno, in relazione alla natura fisica e chimica del materiale (struttura delle fasi, composizione chimica, rugosità superficiale del pezzo, sollecitazioni residue e di esercizio nel materiale e altro);
- esterno (condizioni ambientali, velocità di movimento di un mezzo corrosivo, temperatura, composizione dell'atmosfera, presenza di inibitori o stimolanti e altro);
- meccanico (sviluppo di cricche da corrosione, distruzione del metallo sotto l'azione di carichi ciclici,cavitazione e corrosione da fretting);
- caratteristiche di progettazione (selezione del tipo di metallo, spazi tra le parti, requisiti di rugosità).
Proprietà fisiche e chimiche
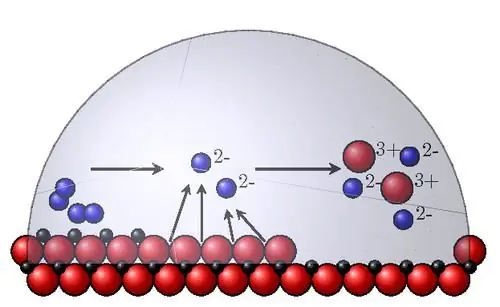
I fattori di corrosione interna più importanti sono i seguenti:
- Stabilità termodinamica. Per determinarlo in soluzioni acquose si utilizzano i diagrammi di Pourbaix di riferimento, lungo l'asse delle ascisse di cui è tracciato il pH del mezzo, e lungo l'asse delle ordinate, il potenziale redox. Un potenziale spostamento nella direzione positiva significa una maggiore stabilità del materiale. Provvisoriamente, è definito come il normale potenziale di equilibrio del metallo. In re altà, i materiali si corrodono a velocità diverse.
- La posizione di un atomo nella tavola periodica degli elementi chimici. I metalli più suscettibili alla corrosione sono i metalli alcalini e alcalino terrosi. Il tasso di corrosione diminuisce all'aumentare del numero atomico.
- Struttura in cristallo. Ha un effetto ambiguo sulla distruzione. La stessa struttura a grana grossa non porta ad un aumento della corrosione, ma è favorevole allo sviluppo della distruzione selettiva intergranulare dei bordi del grano. I metalli e le leghe con distribuzione omogenea delle fasi si corrodono in modo uniforme, mentre quelli con distribuzione non uniforme si corrodono secondo un meccanismo focale. La disposizione reciproca delle fasi svolge la funzione di anodo e catodo in un ambiente aggressivo.
- Disomogeneità energetica degli atomi nel reticolo cristallino. Gli atomi con la massima energia si trovano agli angoli delle faccemicrorugosità e sono centri attivi di dissoluzione durante la corrosione chimica. Pertanto, un'attenta lavorazione delle parti metalliche (levigatura, lucidatura, finitura) aumenta la resistenza alla corrosione. Questo effetto si spiega anche con la formazione di film di ossido più densi e continui su superfici lisce.
Influenza della media acidità

Nel processo di corrosione chimica, la concentrazione di ioni idrogeno influisce sui seguenti punti:
- solubilità dei prodotti di corrosione;
- formazione di film di ossido protettivo;
- Tasso di distruzione dei metalli.
Quando il pH è compreso tra 4 e 10 unità (soluzione acida), la corrosione del ferro dipende dall'intensità della penetrazione dell'ossigeno sulla superficie dell'oggetto. Nelle soluzioni alcaline, la velocità di corrosione diminuisce prima a causa della passivazione superficiale, quindi, a pH >13, aumenta a causa della dissoluzione del film di ossido protettivo.
Per ogni tipo di metallo c'è una propria dipendenza dell'intensità della distruzione dall'acidità della soluzione. I metalli nobili (Pt, Ag, Au) sono resistenti alla corrosione in un ambiente acido. Zn, Al vengono rapidamente distrutti sia negli acidi che negli alcali. Ni e Cd sono resistenti agli alcali ma si corrodono facilmente negli acidi.
Composizione e concentrazione di soluzioni neutre

Il tasso di corrosione in soluzioni neutre dipende maggiormente dalle proprietà del sale e dalla sua concentrazione:
- Durante l'idrolisi dei sali inin un ambiente corrosivo si formano ioni che agiscono come attivatori o ritardatori (inibitori) della distruzione dei metalli.
- Quei composti che aumentano il pH aumentano anche la velocità del processo distruttivo (ad esempio carbonato di sodio) e quelli che riducono l'acidità la diminuiscono (cloruro di ammonio).
- In presenza di cloruri e solfati nella soluzione, si attiva la distruzione fino al raggiungimento di una certa concentrazione di sali (che si spiega con l'intensificazione del processo anodico sotto l'influenza di ioni cloruro e zolfo), e quindi diminuisce gradualmente a causa di una diminuzione della solubilità dell'ossigeno.
Alcuni tipi di sali sono in grado di formare una pellicola insolubile (ad esempio, fosfato di ferro). Questo aiuta a proteggere il metallo da un'ulteriore distruzione. Questa proprietà viene utilizzata quando si applicano neutralizzatori di ruggine.
Inibitori della corrosione
Gli inibitori della corrosione (o inibitori) differiscono nel loro meccanismo d'azione sul processo redox:
- Anodo. Grazie a loro si forma un film passivo. Questo gruppo comprende composti a base di cromati e bicromati, nitrati e nitriti. L'ultimo tipo di inibitori viene utilizzato per la protezione interoperativa delle parti. Quando si utilizzano inibitori di corrosione anodici, è necessario determinare prima la loro concentrazione protettiva minima, poiché l'aggiunta di piccole quantità può portare ad un aumento del tasso di distruzione.
- Catodo. Il meccanismo della loro azione si basa su una diminuzione della concentrazione di ossigeno e, di conseguenza, su un rallentamento del processo catodico.
- Protezione. Questi inibitori isolano la superficie del metallo formando composti insolubili che si depositano come uno strato protettivo.
L'ultimo gruppo comprende neutralizzatori di ruggine, che vengono utilizzati anche per pulire gli ossidi. Di solito contengono acido fosforico. Sotto la sua influenza si verifica la fosfatazione dei metalli: la formazione di un forte strato protettivo di fosfati insolubili. I neutralizzanti vengono applicati con una pistola a spruzzo o un rullo. Dopo 25-30 minuti la superficie assume un colore bianco-grigio. Dopo che la composizione si asciuga, vengono applicati pitture e vernici.
Azione meccanica

Un aumento della corrosione in un ambiente aggressivo è facilitato da tipi di azione meccanica quali:
- Sforzi interni (durante lo stampaggio o il trattamento termico) ed esterni (sotto l'influenza di un carico applicato esternamente). Di conseguenza, si verifica una disomogeneità elettrochimica, la stabilità termodinamica del materiale diminuisce e si formano crepe da corrosione. Particolarmente veloce è la distruzione sotto carichi di trazione (le crepe si formano su piani perpendicolari) in presenza di anioni ossidanti, ad esempio NaCl. Un tipico esempio di dispositivi soggetti a questo tipo di distruzione sono parti di caldaie a vapore.
- Azione dinamica alternata, vibrazione (fatica da corrosione). C'è un'intensa diminuzione del limite di fatica, si formano più microfessure, che poi si fondono in una grande. Numeroi cicli a cedimento in misura maggiore dipendono dalla composizione chimica e delle fasi di metalli e leghe. Gli assi delle pompe, le molle, le pale delle turbine e altre apparecchiature sono soggetti a tale corrosione.
- Frizione delle parti. La rapida corrosione è dovuta all'usura meccanica delle pellicole protettive sulla superficie del pezzo e all'interazione chimica con l'ambiente. Nel liquido, il tasso di distruzione è inferiore a quello nell'aria.
- Impatto di cavitazione. La cavitazione si verifica quando la continuità del flusso del liquido viene violata a causa della formazione di bolle di vuoto che collassano e creano un effetto pulsante. Di conseguenza, si verifica un danno profondo di natura locale. Questo tipo di corrosione è spesso visto negli apparati chimici.
Fattori di progettazione

Quando si progettano elementi che operano in condizioni aggressive, si deve tenere conto che il tasso di corrosione aumenta nei seguenti casi:
- quando metalli dissimili entrano in contatto (maggiore è la differenza nel potenziale dell'elettrodo tra di loro, maggiore è la forza della corrente del processo elettrochimico di distruzione);
- in presenza di concentratori di sollecitazioni meccaniche (scanalature, scanalature, fori e altro);
- con bassa pulizia della superficie lavorata, in quanto ciò si traduce in coppie galvaniche locali in cortocircuito;
- con una significativa differenza di temperatura delle singole parti dell'apparato (si formano cellule galvaniche termiche);
- in presenza di zone stagnanti (slot, lacune);
- durante la formazionesollecitazioni residue, soprattutto nei giunti saldati (per eliminarle è necessario prevedere un trattamento termico - ricottura).
Metodi di valutazione

Ci sono diversi modi per valutare il tasso di distruzione dei metalli in ambienti aggressivi:
- Laboratorio: test di campioni in condizioni simulate artificialmente vicine al reale. Il loro vantaggio è che ti permettono di ridurre il tempo dello studio.
- Campo - tenuto in condizioni naturali. Ci vogliono molto tempo. Il vantaggio di questo metodo è ottenere informazioni sulle proprietà del metallo nelle condizioni di ulteriore operazione.
- Test in situ di oggetti metallici finiti nell'ambiente naturale.






