Lo stato tridimensionale dell'acqua liquida è difficile da studiare, ma si è imparato molto analizzando la struttura dei cristalli di ghiaccio. Quattro atomi di ossigeno vicini che interagiscono con l'idrogeno occupano i vertici di un tetraedro (tetra=quattro, edro=piano). L'energia media richiesta per rompere un tale legame nel ghiaccio è stimata in 23 kJ/mol-1.

La capacità delle molecole d'acqua di formare un dato numero di catene di idrogeno, oltre a una determinata forza, crea un punto di fusione insolitamente alto. Quando si scioglie, è trattenuto da acqua liquida, la cui struttura è irregolare. La maggior parte dei legami idrogeno sono distorti. Ci vuole una grande quantità di energia sotto forma di calore per rompere il reticolo cristallino del ghiaccio legato all'idrogeno.
Caratteristiche dell'aspetto del ghiaccio (Ih)
Molti abitanti si stanno chiedendo che tipo di reticolo cristallino abbia il ghiaccio. NecessarioVa notato che la densità della maggior parte delle sostanze aumenta durante il congelamento, quando i movimenti molecolari rallentano e si formano cristalli densamente impaccati. Anche la densità dell'acqua aumenta quando si raffredda fino a un massimo di 4°C (277K). Quindi, quando la temperatura scende al di sotto di questo valore, si espande.
Questo aumento è dovuto alla formazione di un cristallo di ghiaccio aperto legato all'idrogeno con il suo reticolo e una densità inferiore, in cui ogni molecola d'acqua è rigidamente vincolata dall'elemento sopra e da altri quattro valori, mentre si muove abbastanza velocemente da avere più massa. Poiché si verifica questa azione, il liquido si congela dall' alto verso il basso. Ciò ha importanti risultati biologici, in conseguenza dei quali lo strato di ghiaccio sullo stagno isola gli esseri viventi dal freddo estremo. Inoltre, due ulteriori proprietà dell'acqua sono legate alle sue caratteristiche dell'idrogeno: calore specifico ed evaporazione.
Descrizione dettagliata delle strutture
Il primo criterio è la quantità necessaria per aumentare di 1°C la temperatura di 1 grammo di una sostanza. L'aumento dei gradi di acqua richiede una quantità di calore relativamente grande perché ogni molecola è coinvolta in numerosi legami a idrogeno che devono essere rotti affinché l'energia cinetica possa aumentare. A proposito, l'abbondanza di H2O nelle cellule e nei tessuti di tutti i grandi organismi multicellulari significa che le fluttuazioni di temperatura all'interno delle cellule sono ridotte al minimo. Questa caratteristica è fondamentale, poiché la velocità della maggior parte delle reazioni biochimichesensibile.
Il calore di vaporizzazione dell'acqua è anche significativamente superiore a quello di molti altri liquidi. È necessaria una grande quantità di calore per convertire questo corpo in un gas, perché i legami idrogeno devono essere rotti affinché le molecole d'acqua si dislocano l'una dall' altra ed entrino in detta fase. I corpi mutevoli sono dipoli permanenti e possono interagire con altri composti simili e quelli che si ionizzano e si dissolvono.
Altre sostanze sopra menzionate possono entrare in contatto solo se è presente la polarità. È questo composto che è coinvolto nella struttura di questi elementi. Inoltre, può allinearsi attorno a queste particelle formate da elettroliti, in modo che gli atomi di ossigeno negativi delle molecole d'acqua siano orientati verso i cationi e gli ioni positivi e gli atomi di idrogeno siano orientati verso gli anioni.
Nei solidi, di regola, si formano reticoli cristallini molecolari e reticoli atomici. Cioè, se lo iodio è costruito in modo tale da contenere I2, , allora nell'anidride carbonica solida, cioè nel ghiaccio secco, le molecole di CO2 sono situato ai nodi del reticolo cristallino . Quando interagisce con sostanze simili, il ghiaccio ha un reticolo cristallino ionico. La grafite, per esempio, che ha una struttura atomica basata sul carbonio, non è in grado di cambiarla, proprio come il diamante.
Cosa succede quando un cristallo di sale da cucina si dissolve in acqua: le molecole polari sono attratte da elementi carichi nel cristallo, il che porta alla formazione di particelle simili di sodio e cloruro sulla sua superficie, risultando in questi corpisono dislocati l'uno dall' altro e inizia a dissolversi. Da qui si può osservare che il ghiaccio ha un reticolo cristallino con legame ionico. Ogni Na + disciolto attira le estremità negative di diverse molecole d'acqua, mentre ogni Cl disciolto attira le estremità positive. Il guscio che circonda ogni ione è chiamato sfera di fuga e di solito contiene diversi strati di particelle di solvente.
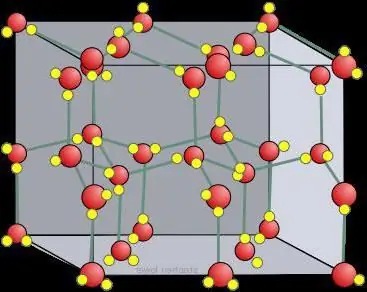
Reticolo cristallino di ghiaccio secco
Si dice che una variabile o uno ione circondato da elementi sia solfato. Quando il solvente è acqua, tali particelle sono idratate. Pertanto, qualsiasi molecola polare tende ad essere solvata dagli elementi del corpo liquido. Nel ghiaccio secco, il tipo di reticolo cristallino forma legami atomici nello stato di aggregazione, che sono invariati. Un' altra cosa è il ghiaccio cristallino (acqua gelata). I composti organici ionici come la carbossilasi e le ammine protonate devono essere solubili nei gruppi idrossile e carbonile. Le particelle contenute in tali strutture si muovono tra le molecole ei loro sistemi polari formano legami idrogeno con questo corpo.
Naturalmente, il numero degli ultimi gruppi indicati in una molecola influisce sulla sua solubilità, che dipende anche dalla reazione di varie strutture nell'elemento: ad esempio, gli alcoli a uno, due e tre atomi di carbonio sono miscibili con acqua, ma gli idrocarburi più grandi con singoli composti idrossilici sono molto meno diluiti nei liquidi.
Hexagonal Ih ha una forma simile areticolo cristallino atomico. Per il ghiaccio e tutta la neve naturale sulla Terra, sembra esattamente così. Ciò è dimostrato dalla simmetria del reticolo cristallino del ghiaccio, cresciuto dal vapore acqueo (cioè dai fiocchi di neve). È nel gruppo spaziale P 63/mm da 194; D 6h, Laue classe 6/mm; simile a β-, che ha un multiplo di 6 assi elicoidali (rotazione intorno oltre a spostamento lungo di esso). Ha una struttura a bassa densità abbastanza aperta in cui l'efficienza è bassa (~1/3) rispetto alle semplici strutture cubiche (~1/2) o cubiche centrate sulla faccia (~3/4).
Rispetto al ghiaccio normale, il reticolo cristallino del ghiaccio secco, legato da molecole di CO2, è statico e cambia solo quando gli atomi decadono.
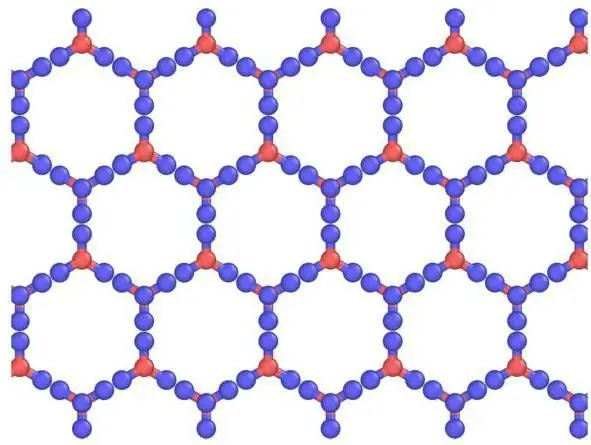
Descrizione dei grigliati e dei loro elementi
I cristalli possono essere visti come modelli cristallini, costituiti da fogli posti uno sopra l' altro. Il legame idrogeno è ordinato, mentre in re altà è casuale, poiché i protoni possono muoversi tra le molecole di acqua (ghiaccio) a temperature superiori a circa 5 K. In effetti, è probabile che i protoni si comportino come un fluido quantistico in un flusso di tunneling costante. Ciò è rafforzato dalla dispersione dei neutroni, che mostra la loro densità di dispersione a metà strada tra gli atomi di ossigeno, indicando la localizzazione e il movimento concertato. Qui c'è una somiglianza del ghiaccio con un reticolo cristallino atomico e molecolare.
Le molecole hanno una disposizione sfalsata della catena dell'idrogenorispetto ai suoi tre vicini nell'aereo. Il quarto elemento ha una disposizione del legame idrogeno eclissato. C'è una leggera deviazione dalla perfetta simmetria esagonale, poiché la cella unitaria è più corta dello 0,3% nella direzione di questa catena. Tutte le molecole sperimentano gli stessi ambienti molecolari. C'è abbastanza spazio all'interno di ogni "scatola" per contenere particelle di acqua interstiziale. Sebbene non siano generalmente considerati, sono stati recentemente rilevati efficacemente dalla diffrazione di neutroni del reticolo cristallino polverulento del ghiaccio.
Cambiare le sostanze
Il corpo esagonale ha punte triple con acqua liquida e gassosa 0,01 °C, 612 Pa, elementi solidi - tre -21,985 °C, 209,9 MPa, undici e due -199,8 °C, 70 MPa, nonché - 34,7 ° C, 212,9 MPa. La costante dielettrica del ghiaccio esagonale è 97,5.
La curva di fusione di questo elemento è data da MPa. Alle equazioni di stato sono disponibili, oltre ad esse, alcune semplici disuguaglianze che mettono in relazione il cambiamento delle proprietà fisiche con la temperatura del ghiaccio esagonale e delle sue sospensioni acquose. La durezza oscilla con gradi che salgono da o sotto il gesso (≦2) a 0°C fino al feldspato (6 Mohs) a -80°C, una variazione anormalmente ampia della durezza assoluta (> 24 volte).
Il reticolo cristallino esagonale di ghiaccio forma piastre e colonne esagonali, dove le facce superiore e inferiore sono i piani basali {0 0 0 1} con un'entalpia di 5,57 μJ cm -2, e altre parti laterali equivalenti sono dette parti del prisma {1 0 -1 0} con 5, 94µJ cm -2. Lungo i piani formati dai lati delle strutture si possono formare superfici secondarie {1 1 -2 0} con 6,90 ΜJ ˣ cm -2.
Tale struttura mostra un'anomala diminuzione della conducibilità termica all'aumentare della pressione (così come ghiaccio cubico e amorfo di bassa densità), ma differisce dalla maggior parte dei cristalli. Ciò è dovuto a un cambiamento nel legame idrogeno, che riduce la velocità trasversale del suono nel reticolo cristallino di ghiaccio e acqua.
Ci sono metodi che descrivono come preparare campioni di cristallo di grandi dimensioni e qualsiasi superficie di ghiaccio desiderata. Si presume che il legame idrogeno sulla superficie del corpo esagonale in studio sarà più ordinato che all'interno del sistema bulk. La spettroscopia variazionale con generazione di frequenza a reticolo di fase ha dimostrato che esiste un'asimmetria strutturale tra i due strati superiori (L1 e L2) nella catena HO sotterranea della superficie basale del ghiaccio esagonale. I legami idrogeno adottati negli strati superiori degli esagoni (L1 O ··· HO L2) sono più forti di quelli accettati nel secondo strato all'accumulo superiore (L1 OH ··· O L2). Strutture di ghiaccio esagonali interattive disponibili.
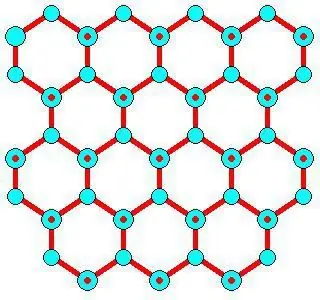
Caratteristiche di sviluppo
Il numero minimo di molecole d'acqua necessarie per formare il ghiaccio è di circa 275 ± 25, come per un ammasso icosaedrico completo di 280. La formazione avviene ad una velocità di 10 10 al interfaccia aria-acqua e non in acqua sfusa. La crescita dei cristalli di ghiaccio dipende da diversi tassi di crescita dei varienergie. L'acqua deve essere protetta dal congelamento durante la crioconservazione di campioni biologici, cibo e organi.
Ciò si ottiene in genere con velocità di raffreddamento elevate, utilizzando piccoli campioni e un crioconservatore e aumentando la pressione per nucleare il ghiaccio e prevenire il danno cellulare. L'energia libera di ghiaccio/liquido aumenta da ~30 mJ/m2 a pressione atmosferica a 40 mJ/m-2 a 200 MPa, indicando motivo per cui si verifica questo effetto.
Che tipo di reticolo cristallino è caratteristico del ghiaccio
In alternativa, possono crescere più velocemente da superfici prismatiche (S2), sulla superficie disturbata casualmente di laghi ghiacciati o agitati. La crescita delle facce {1 1 -2 0} è almeno la stessa, ma le trasforma in basi prismatiche. I dati sullo sviluppo del cristallo di ghiaccio sono stati completamente studiati. I tassi di crescita relativi di elementi di diverse facce dipendono dalla capacità di formare un ampio grado di idratazione articolare. La temperatura (bassa) dell'acqua circostante determina il grado di ramificazione del cristallo di ghiaccio. La crescita delle particelle è limitata dalla velocità di diffusione a un basso grado di superraffreddamento, ovvero <2 °C, con conseguente aumento di esse.

Ma limitato dalla cinetica di sviluppo a livelli di depressione più elevati di >4°C, con conseguente crescita dell'ago. Questa forma è simile alla struttura del ghiaccio secco (ha un reticolo cristallino con una struttura esagonale), variacaratteristiche dello sviluppo della superficie e della temperatura dell'acqua circostante (superraffreddata), che si trova dietro le forme piatte dei fiocchi di neve.
La formazione di ghiaccio nell'atmosfera influenza profondamente la formazione e le proprietà delle nuvole. I feldspati, che si trovano nella polvere del deserto che entra nell'atmosfera in milioni di tonnellate all'anno, sono importanti precursori. Simulazioni al computer hanno dimostrato che ciò è dovuto alla nucleazione di piani prismatici di cristalli di ghiaccio su piani di superficie ad alta energia.
Alcuni altri elementi e reticoli
Le sostanze disciolte (ad eccezione di elio e idrogeno molto piccoli, che possono entrare negli interstizi) non possono essere incluse nella struttura Ih a pressione atmosferica, ma sono spinte verso la superficie o strato amorfo tra le particelle del corpo microcristallino. Ci sono altri elementi nei siti reticolari del ghiaccio secco: ioni caotropici come NH4 + e Cl - che sono inclusi nel congelamento liquido più leggero rispetto ad altri cosmotropici come Na + e SO42-, quindi non è possibile rimuoverli poiché formano una sottile pellicola del liquido rimanente tra i cristalli. Ciò può portare alla carica elettrica della superficie a causa della dissociazione dell'acqua superficiale bilanciando le cariche rimanenti (che possono anche portare a radiazioni magnetiche) e una variazione del pH dei film liquidi residui, ad esempio NH 42SO4 diventa più acido e NaCl diventa più basico.
Sono perpendicolari alle faccereticolo cristallino di ghiaccio che mostra lo strato successivo attaccato (con atomi di O in nero). Sono caratterizzati da una superficie basale a crescita lenta {0 0 0 1}, dove sono attaccate solo molecole d'acqua isolate. Una superficie {1 0 -1 0} in rapida crescita di un prisma in cui coppie di particelle appena attaccate possono legarsi tra loro con idrogeno (un legame idrogeno/due molecole di un elemento). La faccia a crescita più rapida è {1 1 -2 0} (prismatica secondaria), dove catene di particelle appena attaccate possono interagire tra loro mediante legame idrogeno. Una delle sue catene/molecole di elemento è una forma che forma creste che dividono e incoraggiano la trasformazione in due lati del prisma.
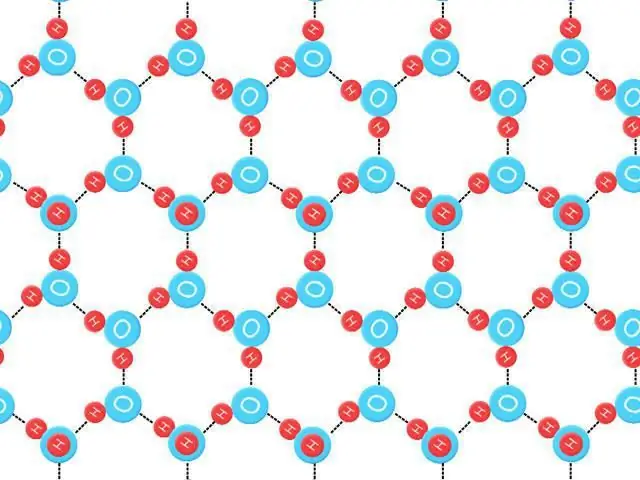
Entropia punto zero
Può essere definito come S 0=k B ˣ Ln (N E0), dove k B è la costante di Boltzmann, NE è il numero di configurazioni all'energia E ed E0 è l'energia più bassa. Questo valore per l'entropia del ghiaccio esagonale a zero Kelvin non viola la terza legge della termodinamica "L'entropia di un cristallo ideale allo zero assoluto è esattamente zero", poiché questi elementi e particelle non sono ideali, hanno legami idrogeno disordinati.
In questo corpo, il legame idrogeno è casuale e cambia rapidamente. Queste strutture non sono esattamente uguali in energia, ma si estendono a un numero molto elevato di stati energeticamente vicini, obbediscono alle "regole del ghiaccio". L'entropia di punto zero è il disordine che rimarrebbe anche se il materiale potesse essere raffreddato all'assolutozero (0 K=-273, 15°C). Genera confusione sperimentale per il ghiaccio esagonale 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. In teoria, sarebbe possibile calcolare l'entropia zero dei cristalli di ghiaccio conosciuti con una precisione molto maggiore (trascurando i difetti e la diffusione del livello di energia) piuttosto che determinarla sperimentalmente.
Gli scienziati e il loro lavoro in quest'area
Può essere definito come S 0=k B ˣ Ln (N E0), dove k B è la costante di Boltzmann, NE è il numero di configurazioni all'energia E ed E0 è l'energia più bassa. Questo valore per l'entropia del ghiaccio esagonale a zero Kelvin non viola la terza legge della termodinamica "L'entropia di un cristallo ideale allo zero assoluto è esattamente zero", poiché questi elementi e particelle non sono ideali, hanno legami idrogeno disordinati.
In questo corpo, il legame idrogeno è casuale e cambia rapidamente. Queste strutture non sono esattamente uguali in energia, ma si estendono a un numero molto elevato di stati energeticamente vicini, obbediscono alle "regole del ghiaccio". L'entropia del punto zero è il disordine che rimarrebbe anche se il materiale potesse essere raffreddato fino allo zero assoluto (0 K=-273,15°C). Genera confusione sperimentale per il ghiaccio esagonale 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. In teoria, sarebbe possibile calcolare l'entropia zero dei cristalli di ghiaccio conosciuti con una precisione molto maggiore (trascurando i difetti e la diffusione del livello di energia) piuttosto che determinarla sperimentalmente.

Sebbene l'ordine dei protoni nel ghiaccio sfuso non sia ordinato, la superficie probabilmente preferisce l'ordine di queste particelle sotto forma di bande di atomi H sospesi e coppie O-single (entropia zero con legami idrogeno ordinati). Si trova il disturbo del punto zero ZPE, J ˣ mol -1 ˣ K -1 e altri. Da tutto quanto sopra, è chiaro e comprensibile quali tipi di reticoli cristallini sono caratteristici del ghiaccio.






