Il mondo in cui viviamo è inimmaginabilmente bello e pieno di molti processi diversi che determinano il corso della vita. Tutti questi processi sono studiati dalla scienza familiare: la fisica. Offre l'opportunità di avere almeno un'idea dell'origine dell'universo. In questo articolo considereremo un concetto come la teoria cinetica molecolare, le sue equazioni, tipi e formule. Tuttavia, prima di passare a uno studio più approfondito di questi problemi, è necessario chiarire a te stesso il significato stesso della fisica e le aree che studia.
Cos'è la fisica?

In effetti, questa è una scienza molto vasta e, forse, una delle più fondamentali nella storia dell'umanità. Ad esempio, se la stessa informatica è associata a quasi ogni area dell'attività umana, che sia la progettazione computazionale o la creazione di cartoni animati, allora la fisica è la vita stessa, una descrizione dei suoi processi e flussi complessi. Proviamo a capirne il significato, semplificando il più possibile la comprensione.
CosìQuindi, la fisica è una scienza che si occupa dello studio dell'energia e della materia, delle connessioni tra di loro, della spiegazione di molti processi che si verificano nel nostro vasto universo. La teoria cinetica molecolare della struttura della materia è solo una piccola goccia nel mare delle teorie e delle branche della fisica.
L'energia, che questa scienza studia in dettaglio, può essere rappresentata in una varietà di forme. Ad esempio, sotto forma di luce, movimento, gravità, radiazione, elettricità e molte altre forme. Toccheremo in questo articolo la teoria cinetica molecolare della struttura di queste forme.
Lo studio della materia ci dà un'idea della struttura atomica della materia. A proposito, segue dalla teoria cinetica molecolare. La scienza della struttura della materia ci permette di comprendere e trovare il significato della nostra esistenza, le ragioni dell'emergere della vita e dell'Universo stesso. Proviamo ancora a studiare la teoria cinetica molecolare della materia.
In primo luogo, sono necessarie alcune introduzioni per comprendere appieno la terminologia e le eventuali conclusioni.
Argomenti di fisica
Rispondendo alla domanda su cosa sia la teoria cinetica molecolare, non si può non parlare di sezioni di fisica. Ognuno di questi si occupa dello studio dettagliato e della spiegazione di un particolare ambito della vita umana. Sono classificati come segue:
- Meccanica, che è divisa in altre due sezioni: cinematica e dinamica.
- Statico.
- Termodinamica.
- Sezione molecolare.
- Elettrodinamica.
- Ottica.
- Fisica dei quanti e nucleo atomico.
Parliamo nello specifico di molecolarefisica, perché si basa sulla teoria cinetica molecolare.
Cos'è la termodinamica?
In generale, la parte molecolare e la termodinamica sono branche strettamente correlate della fisica, che studiano esclusivamente la componente macroscopica del numero totale dei sistemi fisici. Vale la pena ricordare che queste scienze descrivono precisamente lo stato interno dei corpi e delle sostanze. Ad esempio, il loro stato durante il riscaldamento, la cristallizzazione, la vaporizzazione e la condensazione, a livello atomico. In altre parole, la fisica molecolare è la scienza dei sistemi costituiti da un numero enorme di particelle: atomi e molecole.
Sono state queste scienze a studiare le principali disposizioni della teoria cinetica molecolare.
Anche nel corso della seconda media, abbiamo familiarizzato con i concetti di micro e macro mondi, sistemi. Non sarà superfluo aggiornare questi termini nella memoria.
Il micromondo, come possiamo vedere dal suo stesso nome, è composto da particelle elementari. In altre parole, questo è il mondo delle piccole particelle. Le loro dimensioni sono misurate nell'intervallo da 10-18 m a 10-4 m, e il tempo del loro stato attuale può raggiungere sia l'infinito che intervalli sproporzionatamente piccoli, ad esempio 10-20 s.
Il Macromondo considera corpi e sistemi di forme stabili, costituiti da molte particelle elementari. Tali sistemi sono commisurati alla nostra dimensione umana.
Inoltre, esiste un mega mondo. È composto da enormi pianeti, galassie cosmiche e complessi.
Nozioni di baseteoria
Ora che abbiamo ricapitolato un po' e ricordato i termini di base della fisica, possiamo passare direttamente all'argomento principale di questo articolo.
La teoria cinetica-molecolare apparve e fu formulata per la prima volta nel diciannovesimo secolo. La sua essenza sta nel fatto che descrive in dettaglio la struttura di qualsiasi sostanza (più spesso la struttura dei gas che dei corpi solidi e liquidi), sulla base di tre disposizioni fondamentali che sono state raccolte dalle ipotesi di scienziati di spicco come Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov e molti altri.
Le disposizioni principali della teoria cinetica molecolare suonano così:
- Assolutamente tutte le sostanze (indipendentemente dal fatto che siano liquide, solide o gassose) hanno una struttura complessa, costituita da particelle più piccole: molecole e atomi. Gli atomi sono talvolta chiamati "molecole elementari".
- Tutte queste particelle elementari sono sempre in uno stato di movimento continuo e caotico. Ognuno di noi si è imbattuto in una prova diretta di questa proposta, ma, molto probabilmente, non le ha attribuito molta importanza. Ad esempio, abbiamo visto tutti sullo sfondo dei raggi del sole che le particelle di polvere si muovono costantemente in una direzione caotica. Ciò è dovuto al fatto che gli atomi producono spinte reciproche tra loro, trasmettendosi costantemente energia cinetica l'uno all' altro. Questo fenomeno fu studiato per la prima volta nel 1827 e prese il nome dallo scopritore: "Moto browniano".
- Tutte le particelle elementari sono in continua interazione tra lorocerte forze che hanno una roccia elettrica.
Vale la pena notare che un altro esempio che descrive la posizione numero due, che può anche applicarsi, ad esempio, alla teoria cinetica molecolare dei gas, è la diffusione. Lo incontriamo nella vita di tutti i giorni e in molteplici test e controlli, quindi è importante avere un'idea al riguardo.
Prima considera i seguenti esempi:
Il dottore ha accidentalmente versato alcol da una fiaschetta sul tavolo. O forse hai lasciato cadere la tua bottiglia di profumo e si è sparsa sul pavimento.
Perché, in questi due casi, sia l'odore di alcol che l'odore di profumo riempiranno l'intera stanza dopo un po' di tempo, e non solo l'area in cui è stato versato il contenuto di queste sostanze?
La risposta è semplice: diffusione.
Diffusione - che cos'è? Come scorre?

Questo è un processo in cui le particelle che compongono una particolare sostanza (di solito un gas) penetrano nei vuoti intermolecolari di un' altra. Nei nostri esempi sopra si è verificato quanto segue: a causa del movimento termico, cioè continuo e dissociato, le molecole di alcol e/o profumo sono cadute negli interstizi tra le molecole d'aria. A poco a poco, sotto l'influenza della collisione con atomi e molecole d'aria, si sono diffusi nella stanza. A proposito, l'intensità della diffusione, cioè la velocità del suo flusso, dipende dalla densità delle sostanze coinvolte nella diffusione, nonché dall'energia di movimento dei loro atomi e molecole, chiamata cinetica. Maggiore è l'energia cinetica, maggiore è rispettivamente la velocità di queste molecole e l'intensità.
Il processo di diffusione più veloce può essere chiamato diffusione nei gas. Ciò è dovuto al fatto che il gas non è omogeneo nella sua composizione, il che significa che i vuoti intermolecolari nei gas occupano rispettivamente una quantità significativa di spazio e il processo di inserimento di atomi e molecole di una sostanza estranea procede più facilmente e più velocemente.
Questo processo è un po' più lento nei liquidi. La dissoluzione di zollette di zucchero in una tazza di tè è solo un esempio della diffusione di un solido in un liquido.
Ma il tempo più lungo è la diffusione in corpi con una solida struttura cristallina. Questo è esattamente così, perché la struttura dei solidi è omogenea e ha un forte reticolo cristallino, nelle celle di cui vibrano gli atomi del solido. Ad esempio, se le superfici di due barre metalliche vengono pulite bene e poi messe in contatto tra loro, dopo un tempo sufficientemente lungo saremo in grado di rilevare pezzi di un metallo nell' altro e viceversa.
Come ogni altra sezione fondamentale, la teoria di base della fisica è divisa in parti separate: classificazione, tipi, formule, equazioni e così via. Pertanto, abbiamo appreso le basi della teoria cinetica molecolare. Ciò significa che puoi tranquillamente procedere alla considerazione dei singoli blocchi teorici.
Teoria molecolare-cinetica dei gas
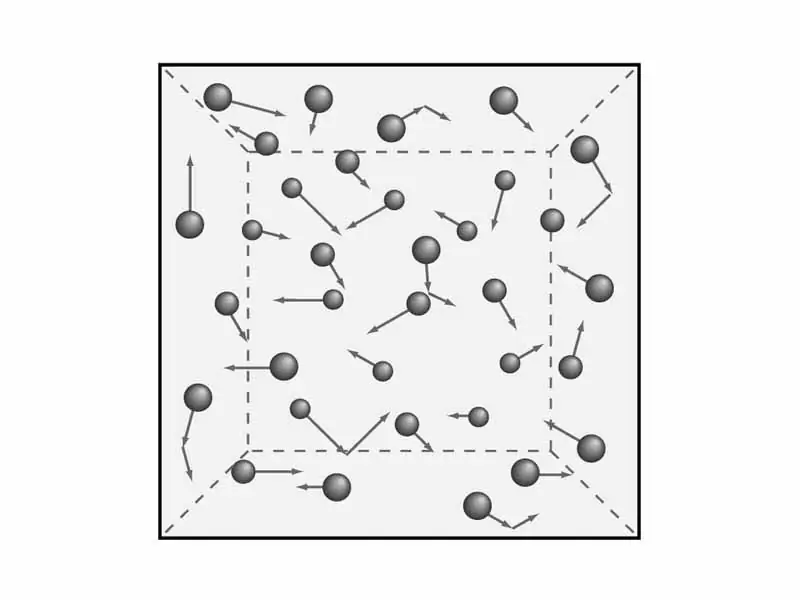
È necessario comprendere le disposizioni della teoria dei gas. Come abbiamo detto in precedenza, considereremo le caratteristiche macroscopiche dei gas, come la pressione e la temperatura. Questo èsarà necessario in seguito per derivare l'equazione della teoria cinetico-molecolare dei gas. Ma la matematica - più tardi, e ora affrontiamo la teoria e, di conseguenza, la fisica.
Gli scienziati hanno formulato cinque disposizioni della teoria molecolare dei gas, che servono a comprendere il modello cinetico dei gas. Suonano così:
- Tutti i gas sono costituiti da particelle elementari che non hanno una certa dimensione, ma hanno una certa massa. In altre parole, il volume di queste particelle è minimo rispetto alla loro lunghezza.
- Gli atomi e le molecole di gas non hanno praticamente energia potenziale, rispettivamente, secondo la legge, tutta l'energia è uguale a quella cinetica.
- Abbiamo già conosciuto questa posizione in precedenza - Moto Browniano. Cioè, le particelle di gas sono sempre in movimento continuo e caotico.
- Assolutamente tutte le collisioni reciproche di particelle di gas, accompagnate dal messaggio di velocità ed energia, sono completamente elastiche. Ciò significa che non vi è alcuna perdita di energia o bruschi s alti nella loro energia cinetica durante una collisione.
- In condizioni normali ea temperatura costante, l'energia media del movimento delle particelle di quasi tutti i gas è la stessa.
Possiamo riscrivere la quinta posizione attraverso questo tipo di equazione della teoria cinetica molecolare dei gas:
E=1/2mv^2=3/2kT, dove k è la costante di Boltzmann; T - temperatura in Kelvin.
Questa equazione ci fa capire la relazione tra la velocità delle particelle elementari di gas e la loro temperatura assoluta. Di conseguenza, maggiore è il loro assolutotemperatura, maggiore è la loro velocità ed energia cinetica.
Pressione del gas
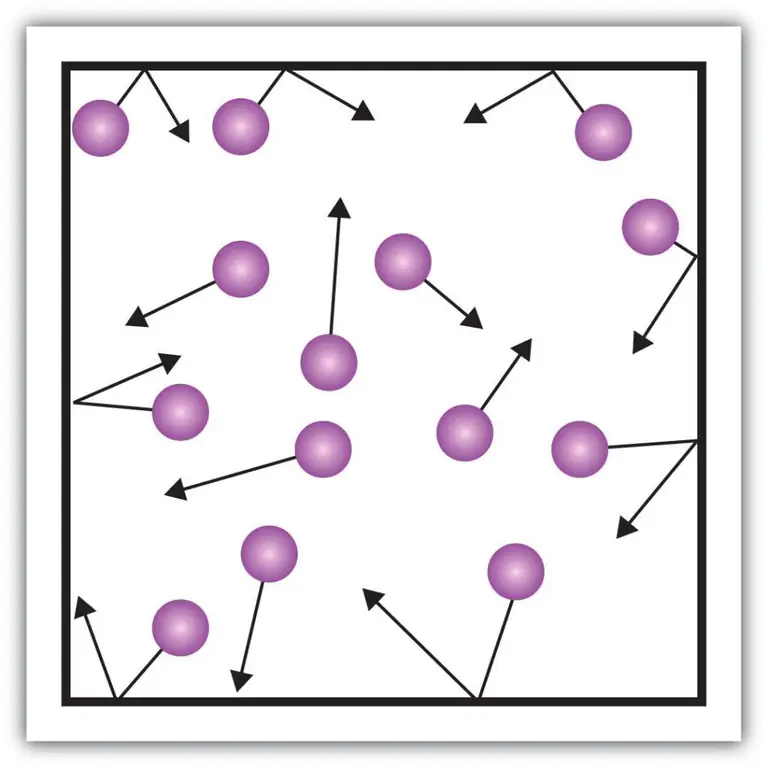
Tali componenti macroscopiche della caratteristica, come la pressione dei gas, possono anche essere spiegate usando la teoria cinetica. Per fare ciò, immaginiamo il seguente esempio.
Assumiamo che una molecola di un gas si trovi in una scatola la cui lunghezza sia L. Usiamo le disposizioni della teoria dei gas sopra descritte e teniamo conto del fatto che la sfera molecolare si muove solo lungo x -asse. Così potremo osservare il processo di collisione elastica con una delle pareti della nave (scatola).
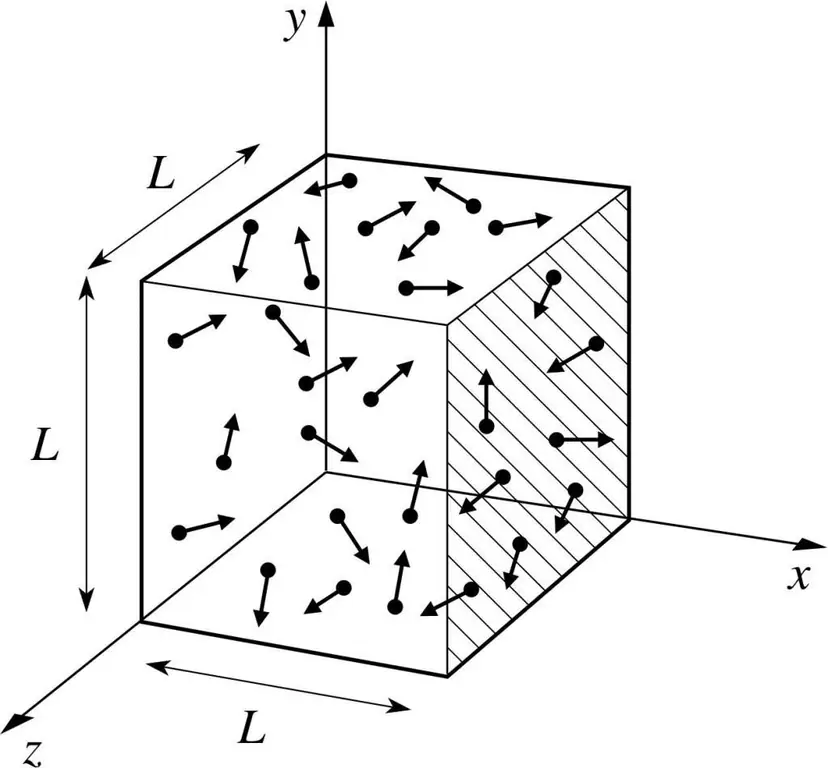
La quantità di moto della collisione in corso, come sappiamo, è determinata dalla formula: p=mv, ma in questo caso questa formula assumerà una forma di proiezione: p=mv(x).
Dato che consideriamo solo la dimensione dell'asse x, cioè l'asse x, la variazione totale della quantità di moto sarà espressa dalla formula: mv(x) - m(-v(x))=2mv(x).
Poi, considera la forza esercitata dal nostro oggetto usando la seconda legge di Newton: F=ma=P/t.
Da queste formule esprimiamo la pressione dal lato gas: P=F/a;
Ora sostituiamo l'espressione di forza nella formula risultante e otteniamo: P=mv(x)^2/L^3.
Dopodiché, la nostra formula di pressione finita può essere scritta per l'N-esimo numero di molecole di gas. In altre parole, sarà simile a questo:
P=Nmv(x)^2/V, dove v è la velocità e V è il volume.
Ora proviamo a mettere in evidenza alcune disposizioni di base sulla pressione del gas:
- Si manifesta attraversocollisioni di molecole con molecole delle pareti dell'oggetto in cui si trova.
- L'entità della pressione è direttamente proporzionale alla forza e alla velocità di impatto delle molecole sulle pareti del recipiente.
Alcune brevi conclusioni sulla teoria
Prima di andare oltre e considerare l'equazione di base della teoria cinetica molecolare, ti offriamo alcune brevi conclusioni dai punti e dalla teoria precedenti:
- La misura dell'energia media di movimento dei suoi atomi e molecole è la temperatura assoluta.
- Quando due diversi gas sono alla stessa temperatura, le loro molecole hanno la stessa energia cinetica media.
- L'energia delle particelle di gas è direttamente proporzionale alla velocità quadratica media: E=1/2mv^2.
- Sebbene le molecole di gas abbiano rispettivamente un'energia cinetica media e una velocità media, le singole particelle si muovono a velocità diverse: alcune veloci, altre lente.
- Più alta è la temperatura, maggiore è la velocità delle molecole.
- Quante volte aumentiamo la temperatura del gas (ad esempio, raddoppia), l'energia di movimento delle sue particelle aumenta tante volte (rispettivamente, raddoppia).
Equazione di base e formule

L'equazione di base della teoria cinetica molecolare permette di stabilire la relazione tra le quantità del micromondo e, di conseguenza, le quantità macroscopiche, cioè misurate.
Uno dei modelli più semplici che la teoria molecolare può considerare è il modello del gas ideale.
Potresti dirloquesto è un tipo di modello immaginario studiato dalla teoria cinetica molecolare di un gas ideale, in cui:
- le particelle di gas più semplici sono considerate come sfere perfettamente elastiche che interagiscono sia tra loro che con le molecole delle pareti di qualsiasi vaso in un solo caso - una collisione assolutamente elastica;
- le forze di attrazione all'interno del gas sono assenti, oppure possono essere addirittura trascurate;
- elementi della struttura interna del gas possono essere presi come punti materiali, cioè anche il loro volume può essere trascurato.
Considerando un tale modello, il fisico di origine tedesca Rudolf Clausius ha scritto una formula per la pressione del gas attraverso la relazione di parametri micro e macroscopici. Sembra:
p=1/3m(0)nv^2.
In seguito questa formula sarà chiamata equazione di base della teoria cinetica molecolare di un gas ideale. Può essere presentato in diverse forme. Il nostro compito ora è mostrare sezioni come la fisica molecolare, la teoria cinetica molecolare e quindi le loro equazioni e tipi completi. Pertanto, ha senso considerare altre variazioni della formula di base.
Sappiamo che l'energia media che caratterizza il moto delle molecole di gas può essere trovata usando la formula: E=m(0)v^2/2.
In questo caso, possiamo sostituire l'espressione m(0)v^2 nella formula della pressione originale con l'energia cinetica media. Di conseguenza, avremo l'opportunità di comporre l'equazione di base della teoria cinetica molecolare dei gas nella seguente forma: p=2/3nE.
Inoltre, sappiamo tutti che l'espressione m(0)n può essere scritta come prodotto di due quozienti:
m/NN/V=m/V=ρ.
Dopo queste manipolazioni, possiamo riscrivere la nostra formula per l'equazione della teoria cinetica molecolare di un gas ideale in una terza forma diversa:
p=1/3ρv^2.
Beh, forse è tutto ciò che devi sapere su questo argomento. Resta solo da sistematizzare le conoscenze acquisite sotto forma di brevi (e non così) conclusioni.
Tutte le conclusioni generali e le formule sull'argomento "Teoria molecolare-cinetica"
Allora iniziamo.
Primo:
La fisica è una scienza fondamentale inclusa nel corso di scienze naturali, che studia le proprietà della materia e dell'energia, la loro struttura, i modelli di natura inorganica.
Include le seguenti sezioni:
- meccanica (cinematica e dinamica);
- statico;
- termodinamica;
- elettrodinamica;
- sezione molecolare;
- ottica;
- fisica dei quanti e del nucleo atomico.
Secondo:
La fisica delle particelle e la termodinamica sono rami strettamente correlati che studiano la componente esclusivamente macroscopica del numero totale di sistemi fisici, cioè i sistemi costituiti da un numero enorme di particelle elementari.
Si basano sulla teoria cinetica molecolare.
Terzo:
Il nocciolo della questione è questo. La teoria cinetica molecolare descrive in dettaglio la struttura di una sostanza (più spesso la struttura dei gas che dei solidi).e corpi liquidi), sulla base di tre ipotesi fondamentali che sono state raccolte dalle ipotesi di eminenti scienziati. Tra questi: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov e molti altri.
Quarto:
Tre principi di base della teoria cinetica molecolare:
- Tutte le sostanze (indipendentemente dal fatto che siano liquide, solide o gassose) hanno una struttura complessa costituita da particelle più piccole: molecole e atomi.
- Tutte queste semplici particelle sono in continuo movimento caotico. Esempio: moto browniano e diffusione.
- Tutte le molecole in qualsiasi condizione interagiscono tra loro con determinate forze che hanno una roccia elettrica.
Ognuna di queste disposizioni della teoria cinetica molecolare è una solida base nello studio della struttura della materia.
Quinto:
Diversi punti principali della teoria molecolare per il modello dei gas:
- Tutti i gas sono costituiti da particelle elementari che non hanno una certa dimensione, ma hanno una certa massa. In altre parole, il volume di queste particelle è minimo rispetto alle distanze tra loro.
- Gli atomi e le molecole di gas non hanno praticamente energia potenziale, rispettivamente la loro energia totale è uguale a quella cinetica.
- Abbiamo già conosciuto questa posizione in precedenza - Moto Browniano. Cioè, le particelle di gas sono sempre in movimento continuo e casuale.
- Assolutamente tutte le collisioni reciproche di atomi e molecole di gas, accompagnate dal messaggio di velocità ed energia, sono completamente elastiche. Questo èsignifica che non vi è alcuna perdita di energia o bruschi s alti nella loro energia cinetica durante una collisione.
- In condizioni normali ea temperatura costante, l'energia cinetica media di quasi tutti i gas è la stessa.
Sesto:
Conclusioni dalla teoria sui gas:
- La temperatura assoluta è una misura dell'energia cinetica media dei suoi atomi e molecole.
- Quando due diversi gas sono alla stessa temperatura, le loro molecole hanno la stessa energia cinetica media.
- L'energia cinetica media delle particelle di gas è direttamente proporzionale alla velocità quadratica media della radice: E=1/2mv^2.
- Sebbene le molecole di gas abbiano rispettivamente un'energia cinetica media e una velocità media, le singole particelle si muovono a velocità diverse: alcune veloci, altre lente.
- Più alta è la temperatura, maggiore è la velocità delle molecole.
- Quante volte aumentiamo la temperatura del gas (ad esempio, il doppio), anche l'energia cinetica media delle sue particelle aumenta tante volte (rispettivamente, il doppio).
- Il rapporto tra la pressione di un gas sulle pareti del recipiente in cui si trova e l'intensità degli impatti delle molecole su queste pareti è direttamente proporzionale: più impatti, maggiore è la pressione, e viceversa.
Settimo:
Un modello di gas ideale è un modello in cui devono essere soddisfatte le seguenti condizioni:
- Le molecole di gas possono e sono considerate come sfere perfettamente elastiche.
- Queste palline possono interagire tra loro e con le pareti di qualsiasinave in un solo caso - collisione assolutamente elastica.
- Quelle forze che descrivono la spinta reciproca tra atomi e molecole di un gas sono assenti o possono essere effettivamente trascurate.
- Gli atomi e le molecole sono considerati punti materiali, cioè anche il loro volume può essere trascurato.
Ottava:
Diamo tutte le equazioni di base e mostriamo le formule nell'argomento "Teoria molecolare-cinetica":
p=1/3m(0)nv^2 - l'equazione di base per il modello del gas ideale, derivata dal fisico tedesco Rudolf Clausius.
p=2/3nE - l'equazione di base della teoria cinetica molecolare di un gas ideale. Derivato dall'energia cinetica media delle molecole.
р=1/3ρv^2 - la stessa equazione, ma considerata attraverso la densità e la velocità quadratica media della radice delle molecole di gas ideali.
m(0)=M/N(a) - la formula per trovare la massa di una molecola attraverso il numero di Avogadro.
v^2=(v(1)+v(2)+v(3)+…)/N - formula per trovare la velocità quadratica media delle molecole, dove v(1), v(2), v (3) e così via - la velocità della prima molecola, della seconda, della terza e così via fino all'ennesima molecola.
n=N/V - formula per trovare la concentrazione di molecole, dove N è il numero di molecole in un volume di gas ad un dato volume V.
E=mv^2/2=3/2kT - formule per trovare l'energia cinetica media delle molecole, dove v^2 è la velocità quadratica media delle molecole, k è una costante valore che prende il nome dall'austriaco la fisica di Ludwig Boltzmann, e T è la temperatura del gas.
p=nkT - formula della pressione in termini di concentrazione, costanteBoltzmann e la temperatura assoluta T. Da essa segue un' altra formula fondamentale, scoperta dallo scienziato russo Mendeleev e dal fisico-ingegnere francese Claiperon:
pV=m/MRT, dove R=kN(a) è la costante universale per i gas.
Ora mostriamo le costanti per diversi isoprocessi: isobarico, isocoro, isotermico e adiabatico.
pV/T=const - eseguita quando la massa e la composizione del gas sono costanti.
рV=const - se anche la temperatura è costante.
V/T=const - se la pressione del gas è costante.
p/T=const - se il volume è costante.
Forse è tutto ciò che devi sapere su questo argomento.
Oggi ci siamo tuffati in un campo scientifico come la fisica teorica, le sue molteplici sezioni e blocchi. Più in dettaglio, abbiamo toccato un'area della fisica come la fisica molecolare fondamentale e la termodinamica, ovvero la teoria cinetica molecolare, che, a quanto pare, non presenta alcuna difficoltà nello studio iniziale, ma in re altà presenta molte insidie. Espande la nostra comprensione del modello del gas ideale, che abbiamo anche studiato in dettaglio. Inoltre, vale la pena notare che abbiamo anche preso dimestichezza con le equazioni di base della teoria molecolare nelle loro varie variazioni e considerato anche tutte le formule più necessarie per trovare determinate incognite su questo argomento, ciò sarà particolarmente utile quando ci si prepara a scrivere qualsiasi prova, esame e prova, o per ampliare la prospettiva generale e la conoscenza della fisica.
Ci auguriamo che questo articolo ti sia stato utile e che tu abbia estratto da esso solo le informazioni più necessarie, rafforzando le tue conoscenze su tali pilastri della termodinamica come le disposizioni di base della teoria cinetica molecolare.






