Gas ideale, equazione di stato del gas ideale, sua temperatura e pressione, volume… l'elenco dei parametri e delle definizioni utilizzati nella corrispondente sezione di fisica può essere continuato per un periodo piuttosto lungo. Oggi parleremo solo di questo argomento.
Cosa viene considerato in fisica molecolare?

L'oggetto principale considerato in questa sezione è un gas ideale. L'equazione di stato del gas ideale è stata ottenuta tenendo conto delle normali condizioni ambientali e di questo ne parleremo un po 'più tardi. Ora affrontiamo questo "problema" da lontano.
Diciamo di avere una massa di gas. Il suo stato può essere determinato utilizzando tre parametri di natura termodinamica. Questi sono, ovviamente, pressione, volume e temperatura. L'equazione dello stato del sistema in questo caso sarà la formula per la relazione tra i parametri corrispondenti. Si presenta così: F (p, V, T)=0.
Qui, per la prima volta, ci stiamo avvicinando lentamente all'emergere di una cosa come l'idealegas. Si chiama gas in cui le interazioni tra le molecole sono trascurabili. In generale, questo non esiste in natura. Tuttavia, qualsiasi gas altamente rarefatto è vicino ad esso. Azoto, ossigeno e aria, che si trovano in condizioni normali, differiscono poco dall'ideale. Per scrivere l'equazione di stato di un gas ideale, possiamo usare la legge unificata dei gas. Otteniamo: pV/T=cost.
Concetto correlato 1: la legge di Avogadro
Può dirci che se prendiamo lo stesso numero di moli di qualsiasi gas a caso e li mettiamo nelle stesse condizioni, inclusa la temperatura e la pressione, allora i gas occuperanno lo stesso volume. In particolare, l'esperimento è stato condotto in condizioni normali. Ciò significa che la temperatura era di 273,15 Kelvin, la pressione era di un'atmosfera (760 millimetri di mercurio, o 101325 Pascal). Con questi parametri il gas occupava un volume pari a 22,4 litri. Pertanto, possiamo dire che per una mole di qualsiasi gas, il rapporto dei parametri numerici sarà un valore costante. Ecco perché è stato deciso di designare questa cifra con la lettera R e chiamarla costante del gas universale. Quindi, è uguale a 8,31. L'unità è J/molK.
Gas ideale. L'equazione di stato del gas ideale e la sua manipolazione
Proviamo a riscrivere la formula. Per fare ciò, lo scriviamo in questa forma: pV=RT. Successivamente, eseguiamo una semplice azione, moltiplichiamo entrambi i membri dell'equazione per un numero arbitrario di moli. Otteniamo pVu=uRT. Prendiamo in considerazione il fatto che il prodotto del volume molare ela quantità di materia è semplicemente il volume. Ma dopo tutto, il numero di moli sarà contemporaneamente uguale al quoziente della massa e della massa molare. Questo è esattamente come appare l'equazione di Mendeleev-Clapeyron. Dà un'idea chiara di che tipo di sistema si forma un gas ideale. L'equazione di stato per un gas ideale assumerà la forma: pV=mRT/M.
Deduci la formula per la pressione
Facciamo altre manipolazioni con le espressioni ottenute. Per fare ciò, il lato destro dell'equazione di Mendeleev-Clapeyron viene moltiplicato e diviso per il numero di Avogadro. Ora osserviamo attentamente il prodotto della quantità di sostanza per il numero di Avogadro. Questo non è altro che il numero totale di molecole nel gas. Ma allo stesso tempo, il rapporto tra la costante universale dei gas e il numero di Avogadro sarà uguale alla costante di Boltzmann. Pertanto, le formule per la pressione possono essere scritte come segue: p=NkT/V o p=nkT. Qui il simbolo n è la concentrazione di particelle.
Processi gas ideali
Nella fisica molecolare esistono cose come gli isoprocessi. Si tratta di processi termodinamici che avvengono nel sistema a uno dei parametri costanti. In questo caso, anche la massa della sostanza deve rimanere costante. Diamo un'occhiata a loro in modo più specifico. Quindi, le leggi di un gas ideale.
La pressione rimane costante
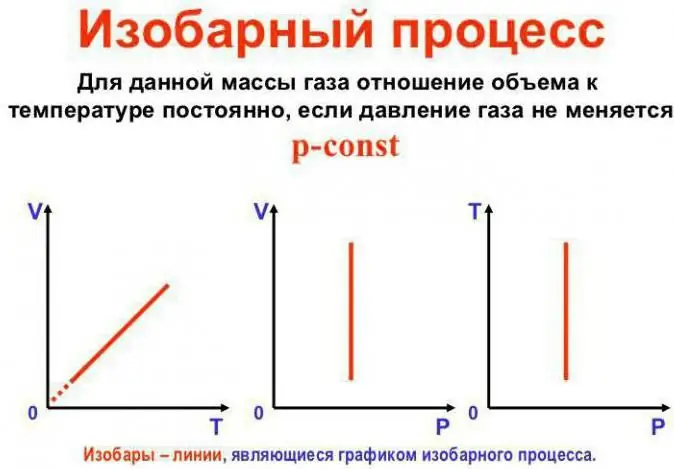
Questa è la legge di Gay-Lussac. Si presenta così: V/T=cost. Può essere riscritto in un altro modo: V=Vo (1 + at). Qui a è uguale a 1/273,15 K^-1 ed è chiamato "coefficiente di espansione del volume". Possiamo sostituire la temperatura sia in Celsius chela scala Kelvin. In quest'ultimo caso, otteniamo la formula V=Voat.
Il volume rimane costante

Questa è la seconda legge di Gay-Lussac, più comunemente chiamata legge di Carlo. Si presenta così: p/T=cost. Esiste un' altra formulazione: p=po (1 + at). Le trasformazioni possono essere eseguite secondo l'esempio precedente. Come puoi vedere, le leggi del gas ideale a volte sono abbastanza simili tra loro.
La temperatura rimane costante

Se la temperatura di un gas ideale rimane costante, allora possiamo ottenere la legge di Boyle-Mariotte. Può essere scritto in questo modo: pV=const.
Concetto correlato n. 2: pressione parziale
Diciamo che abbiamo una nave con dei gas. Sarà una miscela. Il sistema è in uno stato di equilibrio termico e i gas stessi non reagiscono tra loro. Qui N indicherà il numero totale di molecole. N1, N2 e così via, rispettivamente, il numero di molecole in ciascuno dei componenti della miscela. Prendiamo la formula della pressione p=nkT=NkT/V. Può essere aperto per un caso specifico. Per una miscela bicomponente, la formula assumerà la forma: p=(N1 + N2) kT/V. Ma poi si scopre che la pressione totale sarà sommata dalle pressioni parziali di ciascuna miscela. Quindi, sembrerà p1 + p2 e così via. Queste saranno le pressioni parziali.
A cosa serve?
La formula che abbiamo ottenuto indica che la pressione nel sistema proviene da ciascun gruppo di molecole. Per inciso, non dipende altri. D alton ne approfittò nel formulare la legge, poi a lui intitolata: in una miscela in cui i gas non reagiscono chimicamente tra loro, la pressione totale sarà uguale alla somma delle pressioni parziali.






