Lo studio dei processi che si verificano nei sistemi statistici è complicato dalla dimensione minima delle particelle e dal loro numero enorme. È praticamente impossibile considerare ogni particella separatamente, quindi vengono introdotte quantità statistiche: la velocità media delle particelle, la loro concentrazione, la massa delle particelle. La formula che caratterizza lo stato del sistema, tenendo conto dei parametri microscopici, è chiamata equazione di base della teoria cinetica molecolare dei gas (MKT).
Un po' sulla velocità media delle particelle
La determinazione della velocità delle particelle è stata inizialmente effettuata sperimentalmente. Un noto esperimento del curriculum scolastico, condotto da Otto Stern, ha permesso di creare un'idea delle velocità delle particelle. Durante l'esperimento è stato studiato il moto degli atomi d'argento in cilindri rotanti: prima in uno stato stazionario dell'impianto, poi quando ruotava con una certa velocità angolare.
Di conseguenza, è stato riscontrato che la velocità delle molecole d'argento supera la velocità del suono ed è di 500 m/s. Il fatto è piuttosto interessante, poiché è difficile per una persona sentire tali velocità di movimento delle particelle nelle sostanze.
Gas ideale
Continua la ricercaSembra possibile solo in un sistema i cui parametri possono essere determinati da misurazioni dirette utilizzando strumenti fisici. La velocità si misura con un tachimetro, ma l'idea di attaccare un tachimetro a una singola particella è assurda. È possibile misurare direttamente solo un parametro macroscopico associato al movimento delle particelle.
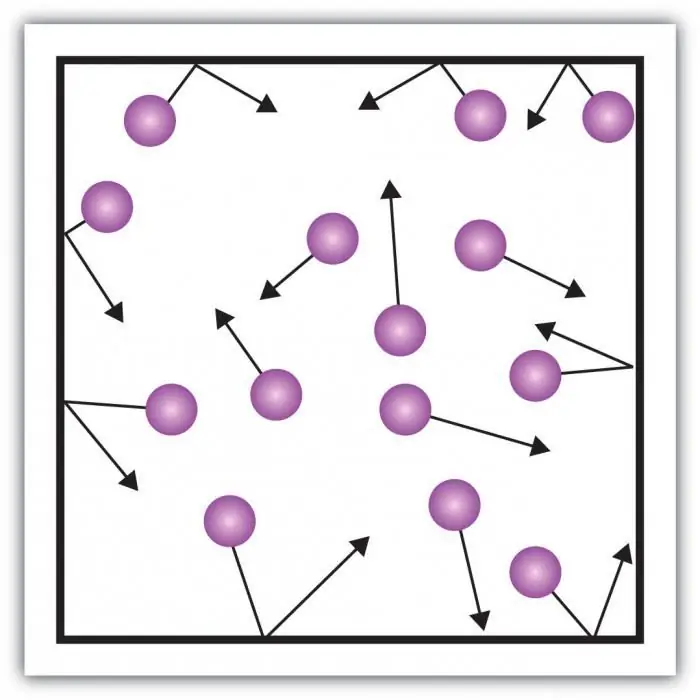
Considera la pressione del gas. La pressione sulle pareti del recipiente è creata dagli impatti delle molecole del gas nel recipiente. La particolarità dello stato gassoso della materia sta nelle distanze sufficientemente grandi tra le particelle e nella loro piccola interazione tra loro. Ciò consente di misurare direttamente la sua pressione.
Qualsiasi sistema di corpi interagenti è caratterizzato da energia potenziale ed energia cinetica di movimento. Il vero gas è un sistema complesso. La variabilità dell'energia potenziale non si presta alla sistematizzazione. Il problema può essere risolto introducendo un modello che porti le proprietà caratteristiche del gas, spazzando via la complessità dell'interazione.
Il gas ideale è uno stato della materia in cui l'interazione delle particelle è trascurabile, l'energia potenziale di interazione tende a zero. Solo l'energia del movimento, che dipende dalla velocità delle particelle, può essere considerata significativa.
Pressione del gas ideale
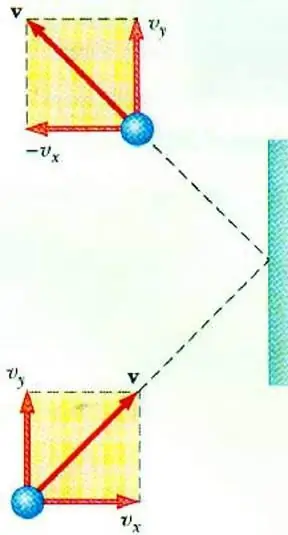
Rivelare la relazione tra la pressione del gas e la velocità delle sue particelle permette l'equazione di base dell'MKT di un gas ideale. Una particella che si muove in un vaso, all'impatto con il muro, gli trasferisce un impulso il cui valore può essere determinato in base alla seconda leggeNewton:
FA∆t=2m0vx
Il cambiamento nella quantità di moto di una particella durante l'impatto elastico è associato a un cambiamento nella componente orizzontale della sua velocità. F è la forza che agisce dal lato della particella sulla parete per un breve tempo t; m0 - massa delle particelle.
Tutte le particelle di gas entrano in collisione con la superficie dell'area S durante il tempo ∆t, muovendosi in direzione della superficie con velocità vx e si trovano in un cilindro di volume Sυ x Δt. Alla concentrazione di particelle n, esattamente metà delle molecole si muove verso la parete, l' altra metà si muove nella direzione opposta.
Dopo aver considerato la collisione di tutte le particelle, possiamo scrivere la legge di Newton per la forza che agisce sull'area:
FA∆t=nm0vx2S∆t
Poiché la pressione del gas è definita come il rapporto tra la forza che agisce perpendicolarmente alla superficie e l'area di quest'ultima, possiamo scrivere:
p=FA: S=nm0vx2
La relazione risultante come equazione di base del MKT non può descrivere l'intero sistema, poiché viene considerata solo una direzione di movimento.
Distribuzione Maxwell
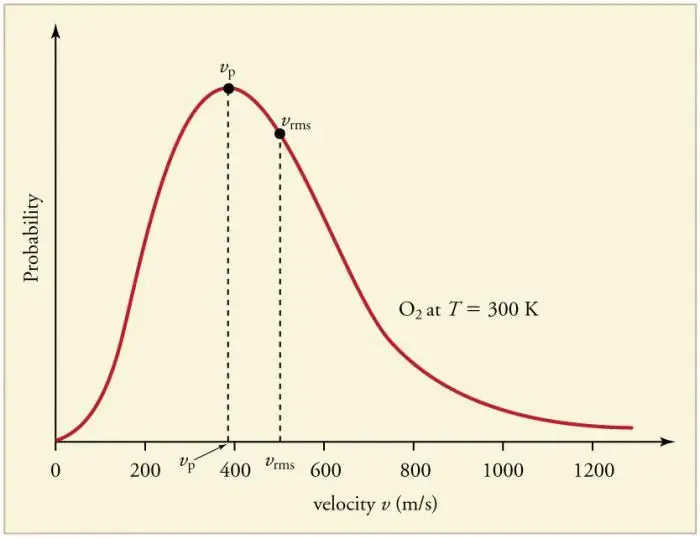
Le continue collisioni frequenti di particelle di gas con le pareti e tra di loro portano all'instaurazione di una certa distribuzione statistica delle particelle in termini di velocità (energie). Le direzioni di tutti i vettori di velocità risultano ugualmente probabili. Questa distribuzione è chiamata distribuzione di Maxwell. Nel 1860 questo modello eraderivato da J. Maxwell sulla base del MKT. I parametri principali della legge di distribuzione sono detti velocità: probabile, corrispondente al valore massimo della curva, e radice quadrata vkv=√‹v2 › - il quadrato medio della velocità delle particelle.
L'aumento della temperatura del gas corrisponde all'aumento della velocità.
Sulla base del fatto che tutte le velocità sono uguali e i loro moduli hanno lo stesso valore, possiamo assumere:
‹v2›=‹vx2› + ‹v y2› + ‹vz2›, da: ‹ vx2›=‹v2›: 3
L'equazione di base dell'MKT, tenendo conto del valore medio della pressione del gas, è:
p=nm0‹v2›: 3.
Questa relazione è unica in quanto determina la relazione tra parametri microscopici: velocità, massa delle particelle, concentrazione delle particelle e pressione del gas in generale.
Utilizzando il concetto di energia cinetica delle particelle, l'equazione di base dell'MKT può essere riscritta in modo diverso:
p=2nm0‹v2›: 6=2n‹Ek›: 3
La pressione di un gas è proporzionale al valore medio dell'energia cinetica delle sue particelle.
Temperatura
È interessante notare che per una quantità costante di gas in un recipiente chiuso, si può mettere in relazione la pressione del gas e il valore medio dell'energia di movimento delle particelle. In questo caso, la pressione può essere misurata misurando l'energiaparticelle.
Cosa fare? Quale valore può essere confrontato con l'energia cinetica? La temperatura risulta essere un tale valore.

La temperatura è una misura dello stato termico delle sostanze. Per misurarlo viene utilizzato un termometro, la cui base è l'espansione termica del fluido di lavoro (alcol, mercurio) quando riscaldato. La scala del termometro viene creata sperimentalmente. Di solito, su di esso vengono apposti segni corrispondenti alla posizione del fluido di lavoro durante alcuni processi fisici che si verificano a uno stato termico costante (acqua bollente, ghiaccio che si scioglie). Termometri diversi hanno scale diverse. Ad esempio, Celsius, Fahrenheit.

Scala temperatura universale
I termometri a gas possono essere considerati più interessanti in termini di indipendenza dalle proprietà del fluido di lavoro. La loro scala non dipende dal tipo di gas utilizzato. In un tale dispositivo, si può ipoteticamente individuare la temperatura alla quale la pressione del gas tende a zero. I calcoli mostrano che questo valore corrisponde a -273,15 oC. La scala di temperatura (scala di temperatura assoluta o scala Kelvin) è stata introdotta nel 1848. La possibile temperatura di pressione del gas zero è stata presa come punto principale di questa scala. Un segmento unitario della scala è uguale a un valore unitario della scala Celsius. Sembra più conveniente scrivere l'equazione MKT di base usando la temperatura quando si studiano i processi del gas.
Rapporto tra pressione e temperatura
Empiricamente, puoi verificarloproporzionalità della pressione del gas alla sua temperatura. Allo stesso tempo, si è riscontrato che la pressione è direttamente proporzionale alla concentrazione di particelle:
P=nkT,
dove T è la temperatura assoluta, k è una costante pari a 1.38•10-23J/K.
Il valore fondamentale, che ha un valore costante per tutti i gas, è chiamato costante di Boltzmann.
Confrontando la dipendenza della pressione dalla temperatura e l'equazione di base dei gas MKT, possiamo scrivere:
‹Ek›=3kT: 2
Il valore medio dell'energia cinetica del movimento delle molecole di gas è proporzionale alla sua temperatura. Cioè, la temperatura può servire come misura dell'energia cinetica del movimento delle particelle.






