La conoscenza delle definizioni in fisica è un fattore chiave per risolvere con successo vari problemi fisici. Nell'articolo considereremo cosa si intende per processi isobarici, isocori, isotermici e adiabatici per un sistema di gas ideali.
Gas ideale e sua equazione
Prima di procedere alla descrizione dei processi isobarici, isocori e isotermici, consideriamo cos'è un gas ideale. Sotto questa definizione in fisica considerano un sistema costituito da un numero enorme di particelle adimensionali e non interagenti che si muovono ad alta velocità in tutte le direzioni. Si tratta infatti di uno stato aggregato gassoso della materia, in cui le distanze tra atomi e molecole superano di gran lunga le loro dimensioni e in cui l'energia potenziale di interazione delle particelle viene trascurata a causa della sua piccolezza, rispetto all'energia cinetica.
Lo stato di un gas ideale è la totalità dei suoi parametri termodinamici. I principali sono temperatura, volume e pressione. Indichiamoli rispettivamente con le lettere T, V e P. Negli anni '30 del XIX secoloClapeyron (uno scienziato francese) per primo ha scritto un'equazione che combina i parametri termodinamici indicati all'interno di un'unica uguaglianza. Sembra:
PV=nRT,
dove n e R sono rispettivamente la quantità di sostanze e la costante del gas.
Cosa sono gli isoprocessi nei gas?
Come molti hanno notato, i processi isobarici, isocorici e isotermici usano lo stesso prefisso "iso" nei loro nomi. Significa l'uguaglianza di un parametro termodinamico durante il passaggio dell'intero processo, mentre i parametri rimanenti cambiano. Ad esempio, un processo isotermico indica che, di conseguenza, la temperatura assoluta del sistema viene mantenuta costante, mentre un processo isocoro indica un volume costante.
Gli isoprocessi sono convenienti da studiare, poiché la fissazione di uno dei parametri termodinamici porta a una semplificazione dell'equazione generale dello stato del gas. È importante notare che le leggi del gas per tutti questi isoprocessi sono state scoperte sperimentalmente. La loro analisi ha permesso a Clapeyron di ottenere l'equazione universale ridotta.
Processi isobarici, isocori e isotermici
Scoperta la prima legge per un processo isotermico in un gas ideale. Ora si chiama legge di Boyle-Mariotte. Poiché T non cambia, l'equazione di stato implica l'uguaglianza:
PV=cost.
In altre parole, ogni variazione di pressione nel sistema porta ad una variazione inversamente proporzionale del suo volume, se la temperatura del gas viene mantenuta costante. Il grafico della funzione P(V) èiperbole.
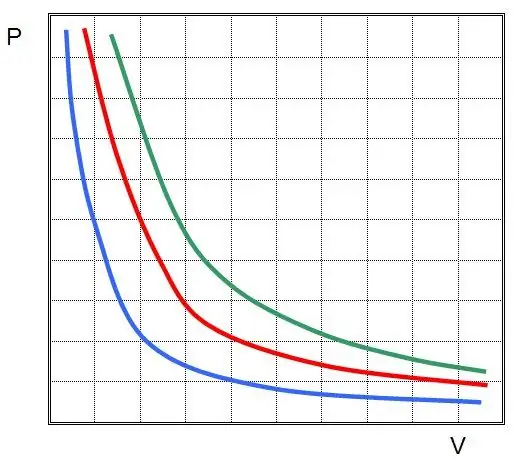
Processo isobarico - questo è un cambiamento nello stato del sistema, in cui la pressione rimane costante. Fissato il valore di P nell'equazione di Clapeyron, otteniamo la seguente legge:
V/T=cost.
Questa uguaglianza porta il nome del fisico francese Jacques Charles, che la ricevette alla fine del XVIII secolo. L'isobar (rappresentazione grafica della funzione V(T)) si presenta come una linea retta. Maggiore è la pressione nel sistema, più velocemente questa linea aumenta.
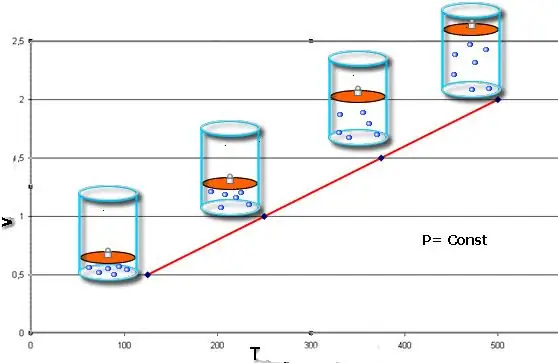
Il processo isobarico è facile da implementare se il gas viene riscaldato sotto il pistone. Le molecole di quest'ultimo aumentano la loro velocità (energia cinetica), creano una maggiore pressione sul pistone, che porta all'espansione del gas e al mantenimento di un valore costante di P.
Infine, il terzo isoprocesso è isocoro. Funziona a volume costante. Dall'equazione di stato otteniamo la corrispondente uguaglianza:
P/T=cost.
E' conosciuta dai fisici come la legge di Gay-Lussac. La diretta proporzionalità tra pressione e temperatura assoluta indica che il grafico del processo isocoro, come il grafico dell'isobarico, è una retta con pendenza positiva.
È importante capire che tutti gli isoprocessi si verificano in sistemi chiusi, cioè il valore di n viene preservato durante il loro corso.
Processo adiabatico
Questo processo non appartiene alla categoria "iso", poiché tutti e tre i parametri termodinamici cambiano durante il suo passaggio. adiabaticochiamato il passaggio tra due stati del sistema, in cui non scambia calore con l'ambiente. Pertanto, l'espansione del sistema viene effettuata a causa delle sue riserve di energia interne, che portano a un calo significativo della pressione e della temperatura assoluta al suo interno.
Il processo adiabatico per un gas ideale è descritto dalle equazioni di Poisson. Uno di questi è mostrato di seguito:
PVγ=const,
dove γ è il rapporto tra le capacità termiche a pressione costante ea volume costante.
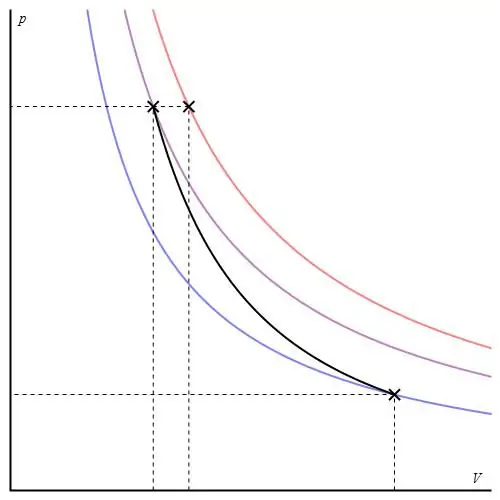
Il grafo adiabatico differisce dal grafo del processo isocoro e dal grafo isobarico, ma è simile a un'iperbole (isoterma). L'adiabat negli assi PV si comporta più bruscamente dell'isoterma.






