Una sezione importante della termodinamica è lo studio delle trasformazioni tra le diverse fasi di una sostanza, poiché questi processi si verificano nella pratica e sono di fondamentale importanza per prevedere il comportamento di un sistema in determinate condizioni. Queste trasformazioni sono dette transizioni di fase, a cui è dedicato l'articolo.
Il concetto di fase e componente di sistema

Prima di procedere alla considerazione delle transizioni di fase in fisica, è necessario definire il concetto di fase stessa. Come è noto dal corso di fisica generale, esistono tre stati della materia: gassoso, solido e liquido. In una sezione speciale della scienza - in termodinamica - le leggi sono formulate per le fasi della materia, e non per i loro stati di aggregazione. Una fase è intesa come un certo volume di materia che ha una struttura omogenea, è caratterizzato da specifiche proprietà fisiche e chimiche ed è separato dal resto della materia da dei limiti, che sono chiamati interfase.
Quindi, il concetto di "fase" porta informazioni molto più praticamente significative sulle proprietàmateria rispetto al suo stato di aggregazione. Ad esempio, lo stato solido di un metallo come il ferro può trovarsi nelle seguenti fasi: cubo centrato sul corpo magnetico a bassa temperatura (BCC), bcc non magnetico a bassa temperatura, cubico centrato sulla faccia (fcc) e temperatura non magnetico bcc.
Oltre al concetto di "fase", le leggi della termodinamica usano anche il termine "componenti", che significa il numero di elementi chimici che compongono un particolare sistema. Ciò significa che la fase può essere monocomponente (1 elemento chimico) o multicomponente (diversi elementi chimici).
Teorema di Gibbs ed equilibrio tra le fasi del sistema

Per comprendere le transizioni di fase, è necessario conoscere le condizioni di equilibrio tra di esse. Queste condizioni possono essere ottenute matematicamente risolvendo il sistema di equazioni di Gibbs per ciascuna di esse, assumendo che lo stato di equilibrio sia raggiunto quando l'energia totale di Gibbs del sistema isolato dall'influenza esterna cessa di cambiare.
Come risultato della risoluzione del sistema di equazioni indicato, si ottengono le condizioni per l'esistenza di equilibrio tra più fasi: un sistema isolato cesserà di evolversi solo quando le pressioni, i potenziali chimici di ogni componente e le temperature in tutte le fasi sono uguali tra loro.
Regola della fase di Gibbs per l'equilibrio

Un sistema composto da più fasi e componenti può essere in equilibrio non soloin determinate condizioni, ad esempio a una temperatura e pressione specifiche. Alcune delle variabili nel teorema di Gibbs per l'equilibrio possono essere modificate mantenendo sia il numero di fasi che il numero di componenti che si trovano in questo equilibrio. Il numero di variabili che possono essere modificate senza disturbare l'equilibrio nel sistema è chiamato numero di libertà di questo sistema.
Il numero di libertà l di un sistema costituito da f fasi e k componenti è determinato in modo univoco dalla regola delle fasi di Gibbs. Questa regola è scritta matematicamente come segue: l + f=k + 2. Come lavorare con questa regola? Molto semplice. Ad esempio, è noto che il sistema è costituito da f=3 fasi di equilibrio. Qual è il numero minimo di componenti che un tale sistema può contenere? Puoi rispondere alla domanda ragionando come segue: nel caso dell'equilibrio, esistono le condizioni più stringenti quando si realizza solo a determinati indicatori, cioè un cambiamento in qualsiasi parametro termodinamico porterà allo squilibrio. Ciò significa che il numero di libertà l=0. Sostituendo i valori noti di l e f, otteniamo k=1, ovvero un sistema in cui tre fasi sono in equilibrio può essere costituito da una componente. Un ottimo esempio è il punto triplo dell'acqua, dove ghiaccio, acqua liquida e vapore esistono in equilibrio a temperature e pressioni specifiche.
Classificazione delle trasformazioni di fase
Se inizi a modificare alcuni parametri termodinamici in un sistema in equilibrio, puoi osservare come una fase scomparirà e ne apparirà un' altra. Un semplice esempio di questo processo è lo scioglimento del ghiaccio quando viene riscaldato.
Dato che l'equazione di Gibbs dipende solo da due variabili (pressione e temperatura), e la transizione di fase comporta un cambiamento di queste variabili, allora matematicamente la transizione tra le fasi può essere descritta differenziando l'energia di Gibbs rispetto alla sua variabili. Fu questo approccio che fu utilizzato dal fisico austriaco Paul Ehrenfest nel 1933, quando compilò una classificazione di tutti i processi termodinamici conosciuti che si verificano con un cambiamento nell'equilibrio di fase.
Dai fondamenti della termodinamica segue che la derivata prima dell'energia di Gibbs rispetto alla temperatura è uguale alla variazione dell'entropia del sistema. La derivata dell'energia di Gibbs rispetto alla pressione è uguale alla variazione di volume. Se, quando le fasi del sistema cambiano, l'entropia o il volume subiscono una rottura, cioè cambiano bruscamente, allora si parla di transizione di fase del primo ordine.
Inoltre, le derivate seconde dell'energia di Gibbs rispetto alla temperatura e alla pressione sono rispettivamente la capacità termica e il coefficiente di espansione volumetrica. Se la trasformazione tra fasi è accompagnata da una discontinuità nei valori delle grandezze fisiche indicate, allora si parla di transizione di fase del secondo ordine.
Esempi di trasformazioni tra fasi

Ci sono un numero enorme di diverse transizioni in natura. Nell'ambito di questa classificazione, esempi sorprendenti di transizioni del primo tipo sono i processi di fusione dei metalli o la condensazione del vapore acqueo dall'aria, quando si verifica un s alto di volume nel sistema.
Se parliamo di transizioni del secondo ordine, allora esempi sorprendenti sono la trasformazione del ferro da uno stato magnetico a uno paramagnetico a una temperatura768 ºC o la trasformazione di un conduttore metallico in uno stato superconduttore a temperature prossime allo zero assoluto.
Equazioni che descrivono transizioni del primo tipo
In pratica, spesso è necessario sapere come cambiano la temperatura, la pressione e l'energia assorbita (rilasciata) in un sistema quando in esso si verificano trasformazioni di fase. A questo scopo vengono utilizzate due equazioni importanti. Si ottengono sulla base della conoscenza delle basi della termodinamica:
- Formula di Clapeyron, che stabilisce il rapporto tra pressione e temperatura durante le trasformazioni tra fasi diverse.
- Formula di Clausius che lega l'energia assorbita (rilasciata) e la temperatura del sistema durante la trasformazione.
L'uso di entrambe le equazioni non è solo per ottenere dipendenze quantitative di grandezze fisiche, ma anche per determinare il segno della pendenza delle curve di equilibrio sui diagrammi di fase.
Equazione per descrivere le transizioni del secondo tipo

Le transizioni di fase del 1° e 2° tipo sono descritte da equazioni diverse, poiché l'applicazione delle equazioni di Clausius e Clausius per le transizioni del secondo ordine porta all'incertezza matematica.
Per descrivere quest'ultimo si utilizzano le equazioni di Ehrenfest, che stabiliscono una relazione tra variazioni di pressione e temperatura attraverso la conoscenza delle variazioni della capacità termica e del coefficiente di espansione volumetrica durante il processo di trasformazione. Le equazioni di Ehrenfest sono usate per descrivere le transizioni conduttore-superconduttore in assenza di campo magnetico.
Importanzadiagrammi di fase
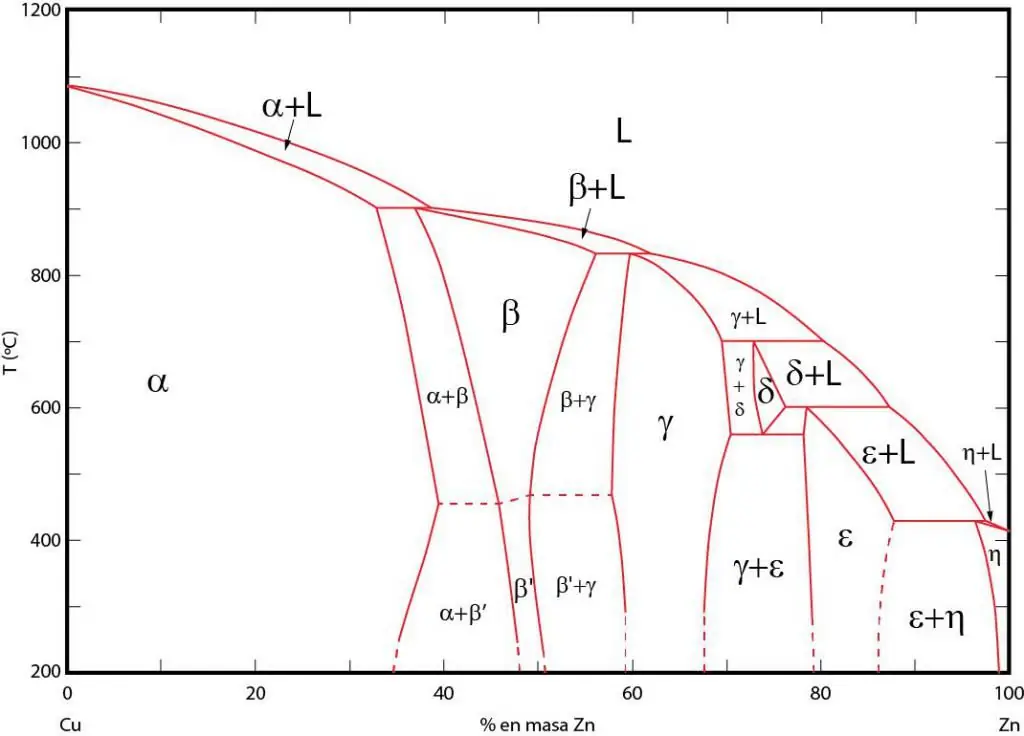
I diagrammi di fase sono una rappresentazione grafica di aree in cui le fasi corrispondenti esistono in equilibrio. Queste aree sono separate da linee di equilibrio tra le fasi. Vengono spesso utilizzati i diagrammi di fase P-T (pressione-temperatura), T-V (temperatura-volume) e PV (pressione-volume).
L'importanza dei diagrammi di fase sta nel fatto che consentono di prevedere in quale fase si troverà il sistema quando le condizioni esterne cambieranno di conseguenza. Queste informazioni vengono utilizzate nel trattamento termico di vari materiali al fine di ottenere una struttura con le proprietà desiderate.






