Quando si studia il comportamento dei gas in fisica, viene prestata molta attenzione agli isoprocessi, ovvero tali transizioni tra gli stati del sistema, durante le quali viene preservato un parametro termodinamico. Tuttavia, c'è una transizione gassosa tra stati, che non è un isoprocesso, ma che svolge un ruolo importante nella natura e nella tecnologia. Questo è un processo adiabatico. In questo articolo, lo considereremo più in dettaglio, concentrandoci su quale sia l'esponente adiabatico del gas.
Processo adiabatico
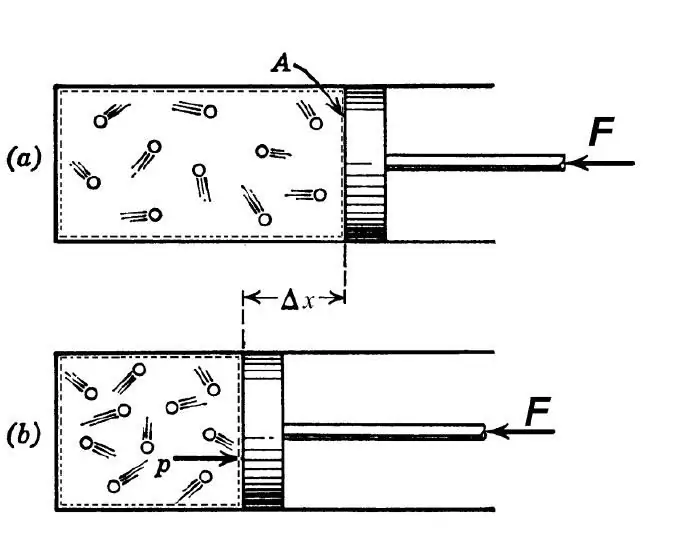
Secondo la definizione termodinamica, per processo adiabatico si intende una tale transizione tra lo stato iniziale e finale del sistema, per cui non vi è scambio termico tra l'ambiente esterno e il sistema in esame. Tale processo è possibile alle seguenti due condizioni:
- conducibilità termica tra l'ambiente esterno eil sistema è basso per un motivo o per l' altro;
- la velocità del processo è elevata, quindi lo scambio termico non ha il tempo di verificarsi.
In ingegneria, la transizione adiabatica viene utilizzata sia per riscaldare il gas durante la sua forte compressione, sia per raffreddarlo durante la rapida espansione. In natura, la transizione termodinamica in questione si manifesta quando una massa d'aria sale o scende dal pendio di una collina. Tali alti e bassi portano a un cambiamento nel punto di rugiada nell'aria e nelle precipitazioni.
Equazione di Poisson per il gas ideale adiabatico

Un gas ideale è un sistema in cui le particelle si muovono casualmente ad alta velocità, non interagiscono tra loro e sono adimensionali. Tale modello è molto semplice in termini di descrizione matematica.
Secondo la definizione di processo adiabatico, secondo la prima legge della termodinamica si può scrivere la seguente espressione:
dU=-PdV.
In altre parole, un gas, in espansione o contrazione, funziona PdV a causa di un corrispondente cambiamento nella sua energia interna dU.
Nel caso di un gas ideale, se utilizziamo l'equazione di stato (legge di Clapeyron-Mendeleev), possiamo ottenere la seguente espressione:
PVγ=cost.
Questa uguaglianza è chiamata equazione di Poisson. Le persone che hanno familiarità con la fisica dei gas noteranno che se il valore di γ è uguale a 1, l'equazione di Poisson entrerà nella legge di Boyle-Mariotte (isotermicaprocessi). Tuttavia, una tale trasformazione delle equazioni è impossibile, poiché γ per qualsiasi tipo di gas ideale è maggiore di uno. La quantità γ (gamma) è chiamata indice adiabatico di un gas ideale. Diamo un'occhiata più da vicino al suo significato fisico.
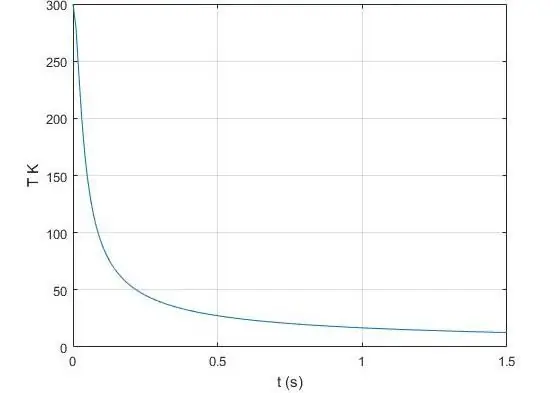
Qual è l'esponente adiabatico?
L'esponente γ, che appare nell'equazione di Poisson per un gas ideale, è il rapporto tra la capacità termica a pressione costante e lo stesso valore, ma già a volume costante. In fisica, la capacità termica è la quantità di calore che deve essere trasferita o prelevata da un dato sistema affinché cambi la sua temperatura di 1 Kelvin. Indicheremo la capacità termica isobarica con il simbolo CP, e la capacità termica isocora con il simbolo CV. Allora vale l'uguaglianza per γ:
γ=CP/CV.
Poiché γ è sempre maggiore di uno, mostra quante volte la capacità termica isobarica del sistema gassoso studiato supera la caratteristica isocora simile.
Capacità termiche di CP e CV
Per determinare l'esponente adiabatico, si dovrebbe avere una buona comprensione del significato delle quantità CP e CV. Per fare ciò, condurremo il seguente esperimento mentale: immagina che il gas si trovi in un sistema chiuso in un recipiente con pareti solide. Se il recipiente è riscaldato, allora tutto il calore comunicato sarà idealmente convertito nell'energia interna del gas. In una tale situazione, l'uguaglianza sarà valida:
dU=CVdT.
ValoreCVdefinisce la quantità di calore che deve essere trasferita al sistema per riscaldarlo isocicamente di 1 K.
Ora supponiamo che il gas sia in un recipiente con un pistone in movimento. Nel processo di riscaldamento di un tale sistema, il pistone si muoverà, garantendo il mantenimento di una pressione costante. Poiché l'entalpia del sistema in questo caso sarà uguale al prodotto della capacità termica isobarica per la variazione di temperatura, la prima legge della termodinamica assumerà la forma:
CPdT=CVdT + PdV.
Da qui si può vedere che CP>CV, poiché nel caso di un cambio di stato isobarico è necessario spendere calore non solo per aumentare la temperatura del sistema, e quindi la sua energia interna, ma anche il lavoro svolto dal gas durante la sua espansione.
Il valore di γ per un gas monoatomico ideale
Il sistema di gas più semplice è un gas ideale monoatomico. Supponiamo di avere 1 mole di un tale gas. Ricordiamo che nel processo di riscaldamento isobarico di 1 mole di gas di solo 1 Kelvin, funziona uguale a R. Questo simbolo è comunemente usato per denotare la costante universale del gas. È uguale a 8, 314 J / (molK). Applicando l'ultima espressione del paragrafo precedente per questo caso, otteniamo la seguente uguaglianza:
CP=CV+ R.
Da dove puoi determinare il valore della capacità termica isocora CV:
γ=CP/CV;
CV=R/(γ-1).
Si sa che per una talpagas monoatomico, il valore della capacità termica isocora è:
CV=3/2R.
Dalle ultime due uguaglianze segue il valore dell'esponente adiabatico:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Si noti che il valore di γ dipende esclusivamente dalle proprietà interne del gas stesso (dalla natura poliatomica delle sue molecole) e non dalla quantità di sostanza nel sistema.
Dipende di γ dal numero di gradi di libertà
L'equazione per la capacità termica isocora di un gas monoatomico è stata scritta sopra. Il coefficiente 3/2 che è apparso in esso è correlato al numero di gradi di libertà in un atomo. Ha la capacità di muoversi solo in una delle tre direzioni dello spazio, cioè ci sono solo gradi di libertà traslazionali.
Se il sistema è formato da molecole biatomiche, ai tre traslazionali vengono aggiunti altri due gradi rotazionali. Pertanto, l'espressione per CV diventa:
CV=5/2R.
Allora il valore di γ sarà:
γ=7/5=1, 4.
Si noti che la molecola biatomica ha effettivamente un grado di libertà vibrazionale in più, ma a temperature di diverse centinaia di Kelvin non si attiva e non contribuisce alla capacità termica.
Se le molecole di gas sono composte da più di due atomi, avranno 6 gradi di libertà. L'esponente adiabatico in questo caso sarà uguale a:
γ=4/3 ≈ 1, 33.
CosìPertanto, all'aumentare del numero di atomi in una molecola di gas, il valore di γ diminuisce. Se costruisci un grafico adiabatico negli assi PV, noterai che la curva per un gas monoatomico si comporterà in modo più netto rispetto a uno poliatomico.
Esponente adiabatico per una miscela di gas
Abbiamo mostrato sopra che il valore di γ non dipende dalla composizione chimica del sistema gassoso. Tuttavia, dipende dal numero di atomi che compongono le sue molecole. Assumiamo che il sistema sia costituito da N componenti. La frazione atomica del componente i nella miscela è ai. Quindi, per determinare l'esponente adiabatico della miscela, puoi usare la seguente espressione:
γ=∑i=1N(aiγ i).
Dove γi è il valore γ per la i-esima componente.
Ad esempio, questa espressione può essere utilizzata per determinare la γ dell'aria. Poiché è costituito per il 99% da molecole biatomiche di ossigeno e azoto, il suo indice adiabatico dovrebbe essere molto vicino al valore di 1,4, che è confermato dalla determinazione sperimentale di questo valore.






